 |
MESURE du pH (1) |
MESURE du pH
Mesurer l'indice pH d'une solution est très facile. C'est une opération fréquente et banale. La mesure avec une sonde électronique est possible.
Qu'est ce que l'indice pH en chimie ?
Toute solution chimique a un certain degré d'acidité qui est fonction de la concentration du cation hydrogène dans la solution.
Plus le nombre d'ions est important, plus l'acidité de la solution est élevée.
Si le nombre d'ions est très faible, on est alors en présence d'une solution basique. ( Voir ACIDE et BASE).
Les concentrations en ions hydrogène étant très différentes d'un extrême à l'autre de la gamme entre acidité et base, on doit définir une unité convenable permettant de travailler et de calculer avec des nombres maniables.
L'indice pH s'exprime avec les logarithmes : pH = - log ( H+ ) avec H+ le nombre d'ions d'hydrogène en mole par litre.
| pH | acide | cations d'hydrogène en g/l | concentration relative | exemple |
| 0 | 1,0 | 10 000 000 | acide chlorhydrique à 5%, acide sulfurique pour batterie | |
| 1 | 0,1 | 1 000 000 | acide gastrique | |
| 2 | 0,01 | 100 000 | jus de citron, vinaigre | |
| 3 | 0,001 | 10 000 | jus de fruit, vin | |
| 4 | 0,0001 | 1 000 | bière | |
| 5 | 0,00001 | 100 | café noir | |
| 6 | 0,000001 | 10 | eau de pluie, eau minérale | |
| 7 | neutre | 0,0000001 | 0 | eau déminéralisée, lait frais |
| 8 | 0,00000001 | 10 | solution de soude | |
| 9 | 0,000000001 | 100 | solution de borax | |
| 10 | 0,0000000001 | 1 000 | solution savonneuse | |
| 11 | 0,00000000001 | 10 000 | révélateur photo | |
| 12 | 0,000000000001 | 100 000 | solution de sel ammoniac | |
| 13 | 0,0000000000001 | 1 000 000 | eau de chaux | |
| 14 | basique | 0,00000000000001 | 10 000 000 | soude caustique à 10% |
exemple : pour un pH de 0, on a 1 g d'ions d'hydrogène par litre.
pour un pH de 14, on 1 E-14 g d'ions par litre.
Chaque graduation correspond à un facteur de 10, en montant ou en descendant l'échelle. Un pH de zéro ne correspond pas à zéro ion, mais à une valeur moyenne située entre ACIDE et BASE : NEUTRE, on a convenu que c'est un pH de 7.
La température de mesure du pH est de 25°C. La température a une influence sur la concentration des ions. Suivant la composition de la solution le pH augmente ou diminue avec la température.
Une solution de mesure consiste à prendre un papier indicateur de tournesol ( colorimétrie ). Précision de 0,3 pH.
Une autre solution est électrique, on peut comparer le potentiel d'une électrode à celui d'une autre électrode de référence. L'électrode de mesure est en verre spécial. La mesure consiste à relever une impédance très élevée ( 10 E+12 ohms ).
Le signal fournit varie de -59,1 mV par unité de pH. Il faut contrôler la température de la mesure avec un capteur de température associé.
Principe de la mesure électronique :
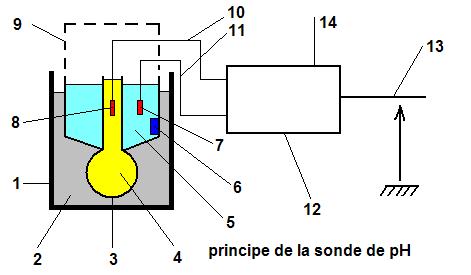
| 1 | récipient contenant la solution à analyser |
| 2 | solution à analyser |
| 3 | membrane de verre |
| 4 | solution tampon |
| 5 | solution tampon |
| 6 | diaphragme |
| 7 | électrode de référence |
| 8 | électrode de conduction |
| 9 | boîtier de la sonde |
| 10 | connexion |
| 11 | connexion |
| 12 | amplificateur soustracteur et inverseur |
| 13 | tension de sortie de 0 à 4 volts |
| 14 | alimentation de l'amplificateur +10 et -10 volts |
L'électrode combinée :
L'électrode combinée est constituée d'une électrode de référence (7) qui fournit une tension électrique constante entre cette électrode et la solution à tester (2). L'électrode de référence (7) est constituée par une électrode d'argent qui baigne dans une solution tampon de chlorure de potassium (5). L'ensemble du fil d'argent et la solution tampon constitue l'électrode de référence.
La solution tampon de l'électrode de référence (5) est en liaison avec la solution à tester par l'intermédiaire d'un diaphragme (6) qui laisse passer un courant extrêmement faible et constitue une faible résistance de transfert. Ce diaphragme est en céramique à pores microscopiques.
L'électrode de conduction est en verre (3), elle est constituée d'une électrode conductrice en argent (8) qui baigne dans une solution tampon (4). L'extrémité est constituée par une membrane de verre (3) d'épaisseur très faible de l'ordre de 0,1 mm. C'est un verre spécial relativement mou.
De part en d'autre de cette membrane se produit une différence de potentiel proportionnelle à la différence entre l'indice d'acidité de la solution tampon à l'intérieur de l'électrode (4) et l'indice d'acidité de la solution à tester (2).
Il est probable qu'elle soit due à un échange d'ions de sodium que contient la solution tampon (4) et d'hydrogène entre le verre (3) et la solution à tester (2).
La différence de potentiel entre les deux électrodes (7) et (8) est en relation linéaire avec la différence de pH entre les deux solutions, celle tampon et celle à mesurer. Les autres tensions électriques présentes dans la chaîne galvanique s'éliminent.
L'impédance d'entrée de l'amplificateur (12) doit être très élevée de l'ordre de 10E12.
La sonde ainsi constituée est très fragile. Elle ne nécessite pas d'entretien particulier. On doit la conserver dans une solution tampon pour éviter son dessèchement.
Le capuchon de la sonde doit contenir une solution de chlorure de potassium à 3 mole/litre pendant le stockage.
Précautions :
Ne jamais toucher la membrane de verre (3) avec les doigts ou avec un autre objet.
Rincer l'électrode avec de l'eau distillée ( pas du robinet ).
Noter la température de la solution pendant toute mesure.
Nettoyer la sonde en cas de tâches sur la membrane (3) avec un produit fourni.
La précision sur la mesure est de 0,02.
Durée de vie de la sonde entre 1 et 3 ans.
Erreurs de mesure aux extrémités de la gamme.
La tension de l'électrode de pH dérive de 200 microvolts par °C. Il faut en tenir compte, d'où une compensation possible.
Etalonnage :
L'étalonnage se fait à l'aide de solutions étalons fournies par le fabriquant de la sonde ( Ingold ). Une solution a pH de 4 et une autre au pH de 7.
On peut étalonner avec une solution au pH de 9, en cas de mesures des solutions basiques.
Critiques :
La sonde est fragile et sa durée de vie est limitée.
Informations plus détaillées :
Pour faire la mesure il faut utiliser deux électrodes. Une électrode de référence dont le potentiel sera pratiquement fixe (7) et une électrode de mesure dont le potentiel sera variable (8).
Electrode de référence au calomel : le calomel est le chlorure de mercure Hg2Cl2
Hg2Cl2 <-- --> 2Hg+ + 2Cl- avec [Hg+].[Cl-] = Ks # 10E-9,7
Hg <-- --> Hg+ + e- avec E° = 0,851 V
Le potentiel de l'électrode est donc fixé par la concentration de la solution tampon dans lequel elle baigne, le chlorure de potassium : K Cl
Electrode de référence au chlorure d'argent :
AgCl <-- --> Ag+ + Cl- avec [Ag+] . [Cl-] = Ks
Ag <-- --> Ag+ + e-
Le potentiel de l'électrode est fixé par la concentration de la solution tampon dans lequel elle baigne, le chlorure de potassium : K Cl
Electrodes de référence et potentiels à 25°C :
| type d'électrode | potentiel E° | Conditions |
| électrodes à hydrogène: H2/H+ | 0,0000 V | pH = 0 Ph2 = 1013,25 hPa |
| électrodes au calomel: Hg2Cl2/Hg/KCl | 0,3337 V | [Cl-] = 0,1 mol/l |
| électrodes au calomel: Hg2Cl2/Hg/KCl | 0,2827 V | [Cl-] = 1 mol/l |
| électrodes au calomel: Hg2Cl2/Hg/KCl | 0,2415 V | solution de KCl saturée |
| électrodes au chlorure d'argent: AgCl/Ag/KCl | 0,2223 V | solution de KCl saturée |
Les électrodes de références peuvent se présenter sous 4 formes :
--- électrolyte liquide, pressurisé ou non
--- électrolyte gélifié
--- électrolyte solide sans diaphragme
--- électrolyte solide et membrane
Dans le cas d'un électrolyte liquide ( KCl ), la jonction électrique entre le couple métallique et la solution est réalisée par l'intermédiaire d'une membrane poreuse en céramique appelée pont d'écoulement ou diaphragme.
Cette membrane peut laisser migrer les ions en solution vers l'électrolyte à moins d'imposer une pression à cet électrolyte. Dans les cas de mesure en cuve à la pression atmosphérique cette mise sous pression est réalisée par la hauteur de liquide d'électrolyte contenue dans un réservoir situé au dessus du niveau libre de la cuve. Il est donc normal d'avoir une baisse de niveau dans la réservoir, un orifice de remplissage permet de faire l'appoint en électrolyte.
L'utilisation d'un gel comme électrolyte de référence, interdit son utilisation lorsque la température ou la pression sont trop élevées. Son emploi est par contre très courant pour les électrodes portables et ne nécessite pas de remplissage.
Pour les électrodes à électrolytes solides ( polymères ), le pont d'écoulement est l'électrolyte lui-même qui pour le cas de celles à membrane PTFE sont gainées de ce matériau. Ces électrodes sont peu sensibles à la migration vers le couple métallique de référence, résistent bien à la pression et à la température et ont un coût et un temps de réponse réduits.
Electrodes idéales :
Il faut un matériel compact facilement transportable et utilisable par un non-chimiste.
Il faut une électrode de mesure assez résistante pour subir des environnements agressifs de température, de pression, de pollution...
Electrodes de verre :
Elle est constituée d'un tube de verre à l'extrémité duquel est soudé une ampoule sphérique ou conique légèrement conductrice. Le tube est rempli d'une solution tampon de pH connu dans laquelle plonge une électrode de mesure. Le potentiel pris par l'électrode est proportionnel au pH de la solution que l'on veut contrôler.
L'électrode de verre a une réponse du genre : tension = a.pH + b
Le terme (a) est la pente de l'électrode et devrait être égal à -0,0591 V.
Cette pente est fonction de la qualité de l'électrode et de son vieillissement. Il faut considérer que cette pente ne doit pas être éloignée de 5% pour être acceptable.
La pente est fonction de la température et il faut effectuer une compensation manuelle ou automatique. Dans ce dernier cas, la sonde de pH est doublée d'une sonde Platine qui indique à l'appareil la température de la solution.
Le tarage ou "standardisation" ou "calibration" consiste à déplacer la courbe de réponse en mesurant le pH de solutions étalons.
Pour ce faire, il faut d'abord régler le zéro qui correspond pour un pH-mètre à un pH de 7.
Quand le zéro est réglé, il faut régler la pente par immersion de la sonde dans une solution de caractéristique connue, par exemple avec un pH de 4 ou de 10 suivant que l'on travaille du côté acide ou du côté basique.

en rouge : réponse avant calibrage
en bleu : calage du zéro à pH = 7
en vert : réponse après ajustement de la pente.
Précautions :
La mesure du pH revient à une mesure de tension. Cette tension est faible de l'ordre de 100 mV. Les électrodes utilisées ont des impédances d'entrées très élevées de 10 à 100 000 Mohms pour des électrodes de verre. Un blindage électrique est nécessaire ( fil blindé ) entre la sonde et l'entrée de l'amplificateur.
Le capteur une fois installé dans la solution nécessite une calibration qui devra être faite à chaque utilisation. Voir la notice du constructeur pour les opérations de calibration ou standardisation : rinçage à l'eau déminéralisée.
Conservation de la sonde en milieu humide ou dans une solution tampon. L'eau de ville peut faire l'affaire. Si la sonde est contaminée, il faut la nettoyer avec une solution recommandée par le constructeur : détergent doux pour corps gras, eau oxygénée...Un nettoyage régulier doit être réalisé avec une solution d'acide chlorhydrique déci molaire pendant une trentaine de minutes suivie d'un bain de 2 heures dans une solution tampon pH7.
Il est formellement déconseillé de toucher ou de heurter les membranes des électrodes, la sonde doit être munie d'une jupe de protection.
Mode opératoire pour la calibration d'une sonde :
--- basculer le pH-mètre en voltmètre.
--- tremper l'électrode de mesure dans une solution tampon de pH=7, relever la tension E1
--- tremper l'électrode de mesure dans une solution tampon de pH=4, relever la tension E2.
E1 doit être telle que : -59 < E1 < +59 mV et E2 - E1 : 159 < E2 < 177 mV
Un bon pH-mètre fournit une précision de pH de + ou - 0,02 pH.
Différents modèles :
chez Conrad : pH mètre CAT, pH-100 ATC, pHT-01 ATC, pH100...
chez Selectronic : AZ8690 pH mètre
voir d'autres sources ....
à suivre,